容量濃度とは何ですか?
1) 容量モル濃度(molarity) 溶液 1 L 中に溶けている溶質の物質量(mol)で表した濃度である。 単位 は mol/L または mol/dm3 を用いる。 単位記号として M(≡mol/L)を用 いることもある。 体積は温度によって変化するので,濃度の表記に体積が含 まれる場合,厳密には温度を記載する。
キャッシュ
濃度と質量パーセント濃度の違いは何ですか?
溶液の「濃度」とは,一定量の溶液に含まれる溶質の量を表したもので,「質量パーセント濃 度」や「モル濃度」がよく使われる。 「質量パーセント濃度」は,溶液の質量のうち溶質がどのくらい含まれているのかという質 量の割合をパーセント[%]で表した濃度で,下図の下にある式で表される。
W/w%と重量%濃度の違いは何ですか?
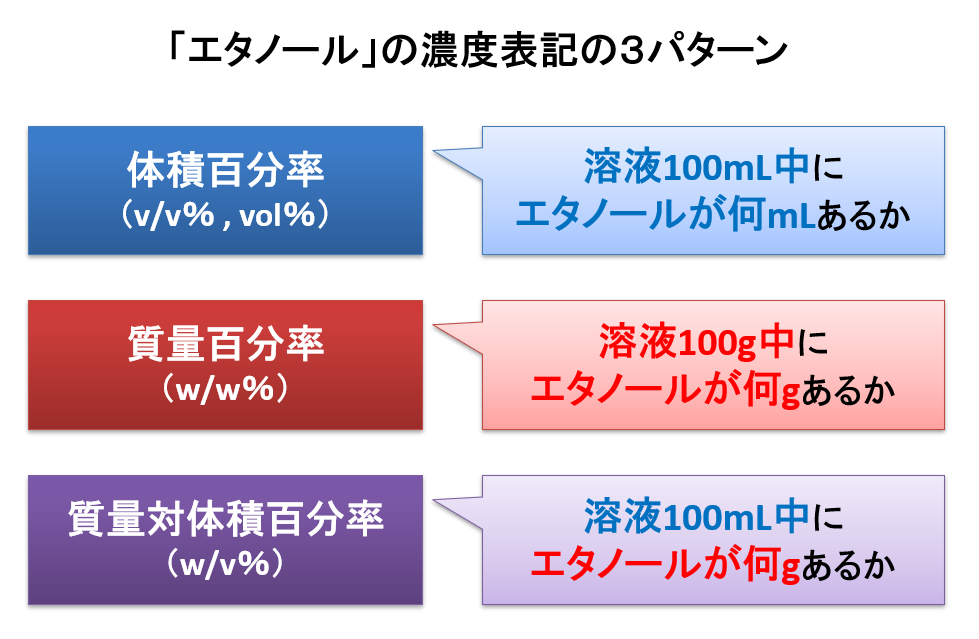
消毒用アルコールをよく見ると「w/w%」などと、アルコールの濃度が記されています。 これは「重量パーセント濃度」の意味。 一方、お酒のボトルに「○度」で表記されている度数は「容量パーセント濃度」を示しています。
キャッシュ
容量モル濃度とは?
molar concentration. 溶液の濃度の表し方の一つ。 普通一定量の溶液中に含まれる溶質のモル数で示す。 溶液の一定量を1000ミリリットルにとったときを容量モル濃度という。
容量モル濃度の求め方は?
モル濃度〔mol/L〕=溶質の物質量〔mol〕/溶液の体積〔L〕
質量パーセント濃度の求め方は?
質量パーセント濃度〔%〕=(溶質の質量〔g〕/溶液の質量〔g〕)×100. 図のように、食塩50gと水200gがあります。
モル濃度 何に使う?
モル濃度は溶液の体積を使うため、温度変化を伴うときは溶液の体積が変化して、モル濃度の数値が変わってしまう。 そこで、温度変化を伴う沸点上昇や凝固点降下のときは質量モル濃度を使う。
%(W/v)とは何ですか?
質量対容量百分率(weight per volume percent)は、溶液100mL中の溶質の質量(g)を表す濃度単位の1つ。 製剤の処方又は成分などを示す場合に用いられる。
重量と容量の違いは何ですか?
それぞれを簡単にいうと、「重量は重さ」、「容量は容器に収めた量」。 この容器というのが計量カップのことです。 「米計量カップ」のすりきりが180㏄(ml)の目盛となりますが、普段、調味料や水の計量に使う計量カップでも同じ目盛で使えます。
モル濃度と容量モル濃度の違いは何ですか?
溶液の濃度の表し方の一つ。 普通一定量の溶液中に含まれる溶質のモル数で示す。 溶液の一定量を1000ミリリットルにとったときを容量モル濃度という。 また溶媒1000グラム中に溶かした溶質のモル数で示したものを質量モル濃度あるいは重量モル濃度という。
質量容量パーセント濃度の求め方は?
質量パーセント濃度〔%〕=(溶質の質量〔g〕/溶液の質量〔g〕)×100.
パーセント濃度の公式は?
質量パーセント濃度〔%〕=(溶質の質量〔g〕/溶液の質量〔g〕)×100. (1)は、質量パーセント濃度を求める問題です。 質量パーセント濃度の求め方を覚えていますか? この式に、溶液の質量200g、溶質の質量4gを当てはめましょう。
質量パーセント濃度 ×100 なぜ?
割合はパーセントで表すことができます。 このパーセントを,百分率といいます。 百分率は全体を100として割合を表すので,パーセントで求めるときには100をかけます。
物質量とモル濃度の違いは何ですか?
物質量は高校で習う化学の中で最初に重要な内容です。 高校化学では様々な場面でこの物質量が出てきます。 「溶液1L中の溶質の量を物質量で表したもの」をモル濃度と言います。 モル濃度のモルは物質量の単位のことです。
1モル濃度とは何ですか?
mol/L(M)という単位で表現されるモル濃度とは、一般的に広く用いられている濃度の表示法で、溶液1リットル中に溶けている目的物質(溶質)のモル数のことです。
容量の単位は?
バイトの単位は、1,024倍ずつ大きくなり、1キロバイト(KB)は1バイトの1,024倍、1メガバイト(MB)は1キロバイトの1,024倍、1ギガバイト(GB)は1メガバイトの1,024倍、1テラバイト(TB)は1ギガバイトの1,024倍になります。
質量パーセント濃度の簡単な求め方は?
質量パーセント濃度〔%〕=(溶質の質量〔g〕/溶液の質量〔g〕)×100.
質量パーセント濃度 なんで100かける?
割合はパーセントで表すことができます。 このパーセントを,百分率といいます。 百分率は全体を100として割合を表すので,パーセントで求めるときには100をかけます。
濃度の調べ方は?
質量パーセント濃度の求め方の公式は、(質量パーセント濃度 [%] )= (溶質の質量)÷(溶液の質量)×100.「溶かした物質の重さ」が「溶けてできた液体全体の重さ」のうち何パーセントをしめるのか?(質量パーセント濃度 [%] )= (溶質の質量)÷(溶液の質量)×100.
1質量パーセントとは何ですか?
概要 「質量パーセント濃度」とは、溶液中の溶質の質量の割合を%で表したもの。 たとえば90gの水に10gの食塩を溶かした場合、溶液全体100gのうち10gが食塩なので 質量パーセント濃度は10% です。


